La Suisse a réservé auprès de la société Moderna, un lot de plus de 4 millions de doses de vaccin anti-SARS-CoV-2, doses qui seraient produites par la firme Lonza, sise dans le Valais. Ce vaccin est fondé sur une technologie innovante dans la production des vaccins. Disons d’emblée que pour un biologiste moléculaire, cette technologie, bien connue et redoutable d’efficacité dans le contexte de la recherche fondamentale en biologie, représente un défi dans le contexte de la vaccinologie. Comme nous sommes prêts à placer nos espoirs dans un tel vaccin, voyons cela de plus près.
La Suisse a réservé auprès de la société Moderna, un lot de plus de 4 millions de doses de vaccin anti-SARS-CoV-2, doses qui seraient produites par la firme Lonza, sise dans le Valais. Ce vaccin est fondé sur une technologie innovante dans la production des vaccins. Disons d’emblée que pour un biologiste moléculaire, cette technologie, bien connue et redoutable d’efficacité dans le contexte de la recherche fondamentale en biologie, représente un défi dans le contexte de la vaccinologie. Comme nous sommes prêts à placer nos espoirs dans un tel vaccin, voyons cela de plus près.
Retour aux fondamentaux. Dans le cadre de la lutte antivirale, la vaccination fait référence à l’acte de présenter à l’organisme cible une version non pathogène du virus, de manière à ce que l’organisme monte une réaction de défense propre à le contenir et à l’éliminer avant apparition de symptômes. Cette réaction de défense se développe en une dizaine de jours après vaccination. Elle est ensuite mise en mémoire pour être réactivée bien plus rapidement après infection. Le vaccin constitue ainsi physiquement une carte d’identité du virus et la vaccination est l’acte permettant de présenter à l’organisme cette identité dans un contexte sans risque.
Bien que les premiers vaccins aient été constitués de version complète du virus (cf. La vaccination) , chimiquement traité pour abolir son pouvoir infectieux (vaccin inactivé) ou sélectionné pour afficher un pouvoir infectieux réduit (vaccin atténué), on a assez tôt réalisé que la présentation à l’organisme d’une fraction de la particule virale suffisait à assurer le succès de la vaccination. Cette fraction se résume en fait à la partie externe du virus, celle exposée à la surface de la particule virale. La vaccination résulte dans ce cadre en la production d’anticorps recouvrant cette partie externe, ce qui provoque l’arrêt du processus d’infection. On est protégé par la présence de ces anticorps, dits neutralisants, dans le sérum. Pour faire simple, préparer un vaccin, selon cette optique, revient à préparer la fraction virale qui va pouvoir être administrée pour susciter la montée des anticorps neutralisants. Dans le meilleur des cas, le vaccin induit également la production et la mise en mémoire de lymphocytes T tueurs de cellules infectées. Comme cet effet est plus compliqué à détecter, l’évidence de l’effet protecteur du vaccin repose généralement sur la seule présence des anticorps neutralisants.
Dans le cas du SARS-CoV-2, la fraction virale se résume à la protéine S qui forme les spicules. La protéine S s’attache au récepteur cellulaire ACE2, ce qui permet au virus, par un jeu subtil de découpage et de contorsions de S d’introduire son génome dans la cellule. Recouvrir la protéine S d’anticorps, c’est empêcher le processus d’infection de se dérouler. Donc préparer un vaccin contre le SARS-CoV-2 se résume à produire la protéine S sous une formulation qui permette sa présentation à l’organisme à vacciner.
On en vient maintenant au cœur de la technologie de production de S. Une nouvelle fois, retour aux fondamentaux. Une protéine, quelle qu’elle soit, est produite sur la base d’une information génétique contenue généralement dans une séquence d’ADN, séquence qui reçoit le nom de gène. On dit qu’un gène exprime une protéine. La protéine S est donc produite suite à l’expression du gène viral S. Si l’on veut disposer de la protéine S pour en faire un vaccin, il faut donc disposer du gène viral S.
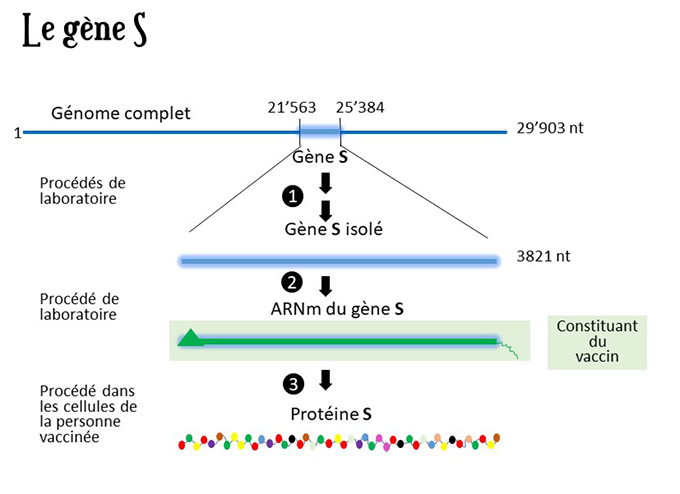
La figure « Le gène S » résume le processus qui mène à la constitution du vaccin ARNm contre le SARS-CoV-2. En première ligne, la connaissance de la séquence complète du génome de SARS-CoV-2, a permis d’identifier la partie du génome qui constitue le gène S. Sur les 29’903 bases (lettres) du génome, 3821 sont dévolues à ce gène, de la position 21’563 à la position 25’384. Il faut donc, dans un premier temps, découper dans le génome, la partie qui correspond à ce gène et l’isoler du reste du génome (Procédé ❶). Par le passé (fin du 20ème siècle), on aurait procédé à un vrai processus de découpage-collage, pour l’obtenir. A l’heure actuelle, on passe commande à une compagnie spécialisée qui livre le gène, synthétisé dans des machines à synthétiser les gènes, contre paiement, cela s’entend.
En possession du gène S, il faut maintenant exprimer ce gène pour obtenir la protéine. L’expression de ce gène se fait, comme pour tout gène, en deux étapes. D’abord la séquence d’ADN est lue par une enzyme, une ARN polymérase, dont la spécialité est de faire une copie ARN de l’ADN du gène (cf. Le génome et L’information génétique). Cet ARN contient la même information que le gène, mais dans une forme qui est intelligible à la machinerie biologique (le ribosome) qui produit la protéine (Procédé ❷). Cet ARN porte le message contenu dans l’ADN, il est dit ARN messager (ARNm). Dans la pratique, l’ARNm du gène S est produit en laboratoire, dans un tube à essai où sont ajoutés au gène S, l’ARN polymérase, plus tout une kyrielle de réactifs
Pour la deuxième étape, à savoir la synthèse de la protéine S à partir de l’ARNm (Procédé ❸), on s’en remet à des cellules dans lesquelles on introduit l’ARNm produit en laboratoire. Ces cellules sont les cellules des personnes qui se trouvent au site d’injection du vaccin. L’ARNm de S, composant du vaccin, induit la synthèse de la protéine S dans les cellules des personnes vaccinées. Le vaccin est injecté sous une forme qui lui permet de traverser les membranes cellulaires pour aboutir, dans les cellules, à l’endroit où les protéines sont synthétisées. L’innovation ici, vient du fait que la protéine S, carte d’identité du virus n’est pas présente dans le vaccin. Le vaccin ne contient que l’ARNm de S, d’où l’appellation de vaccin-ARNm.
- Un des défis de cette approche vient du fait que l’ARN en général, et l’ARNm en particulier, est une molécule extrêmement fragile, cela pour deux raisons. Chimiquement, une réaction qui la brise en morceaux en fonction de la température en fait une entité très instable. Deuxièmement, l’ARN est dégradé très efficacement par des enzymes, les ARNases qui, synthétisées par les bactéries, les champignons, les levures etc., se retrouvent partout, dans les solutions, sur des surfaces, sur les mains, à tel point qu’en laboratoire, qui travaille avec de l’ARN, plonge tous les tubes à essai dans la glace fondante et passe son temps à éviter sa dégradation par les ARNases. Les ARNm-vaccins ont été modifiés chimiquement pour faire face à cette fragilité, mais leur transport va quand même demander des conditions frigorifiques drastiques.
- Un deuxième défi concerne la nécessité pour cet ARNm de pénétrer dans les cellules, car ce n’est qu’à l’intérieur des cellules que l’ARNm produit la protéine S. Or l’ARNm est une grosse molécule chargée négativement qui ne traverse pas spontanément les membranes cellulaires. Il doit être enrobé d’une solution lipidique (graisseuse) qui en se fondant avec les lipides composant les membranes va lui permettre d’atteindre l’intérieur de la cellule. En laboratoire, cette opération, appelée « transfection », est généralement peu efficace. Dans le vaccin, on imagine que les lipides d’enrobement peuvent servir d’adjuvant qui pourrait, en favorisant l’inflammation, compenser la faible efficacité de la transfection.
- Un troisième défi est en relation avec le type d’immunité qui va être déclenché par une tel procédé de vaccination. Dans la vaccination « classique », la carte d’identité du virus « nage » dans le milieu extracellulaire et est présentée intégralement au système immunitaire (lymphocytes B). Dans le cas présent, la carte d’identité n’est produite qu’à l’intérieur des cellules dites « transfectées ». Dans ces conditions on sait que la carte d‘identité est découpée et présentée en fragments. Cette présentation est bien connue dans la phase de la réponse immune fondée sur la présence de lymphocytes tueuses de cellules infectées. Elle ne participe généralement pas à la production d’anticorps neutralisants qui restent, après vaccination, le critère de protection contre l’infection. Pour la production des anticorps, il va falloir compter avec l’expression de la protéine S à la surface des cellules qui la produisent. C’est là qu’elle peut alerter les lymphocytes B, productrices d’anticorps.
Ces défis ont dû être relevés par les concepteurs et les fabricants de ce type de vaccination. Les tests en cours vont nous dire dans quelles mesures les solutions adoptées sont pertinentes.
A l‘énoncé de ces défis, on peut se demander ce qui a poussé les chercheurs à s’engager dans cette voie innovante, alors que les méthodes classiques ou fondées sur des vecteurs viraux on fait leur preuve (cf. Un vaccin pour le SARS-CoV-2). Un aspect ressort qui revêt une importance de premier plan. Si le vaccin ARNm fait ses preuves, il devient une méthode modulable, facilement adaptée à la production d’une variété de protéines virales différentes. Il suffirait de substituer le gène S par le gène produisant la carte d’identité d’un autre virus, nouvellement émergé dans la population humaine, par exemple. Ceci sans se préoccuper des caractéristiques biochimiques de la protéine, car cette dernière se trouve produite au cœur même de l’organisme vacciné, comme le serait la protéine produite après infection. On pourrait étendre l’application de cette technologie à une vaccination contre des cellules cancéreuses, lorsque celles-ci expriment en quantité une protéine particulière. Encore une fois, l’incertitude est de mise. L’avenir nous dira si la méthode du vaccin-ARNm va répondre à nos attentes.
NB. Une entreprise de biotechnologie, BioNTech, en association avec la firme pharmaceutique Pfizer, vient d’annoncer le succès d’un essai de vaccination de phase III dans lequel 90% des personnes vaccinées ont apparemment monté une immunité contre le SARS-CoV2. Ce vaccin, comme celui décrit ci-dessus , est un vaccin à ARNm. Fait intéressant, les chercheurs de BioNTech ont développé cette technologie en pensant surtout à des médicaments pour soigner des cancers. Ce n’est que devant l’urgence sanitaire actuelle qu’ils ont momentanément donné la priorité à la mise au point d’un vaccin antiviral. Cette réalisation, si elle se confirme, peut donc servir de preuve du principe d’une stratégie thérapeutique dans la lutte contre le cancer.
NBB. C’est au tour de Moderna d’annoncer les résultats de phase III de son vaccin. 94% d’efficacité, mais surtout une stabilité qui semble bien supérieure. Stable au frigidaire pendant près de 30 jours pour Moderna, comparé à la nécessité de le conserver à -80°C pour BioNTech.
Publié 04/11/2020
màj 21 août 2025