Le test rapide, dit antigénique, vise à détecter des protéines virales présentes dans un échantillon clinique, servant ainsi de test diagnostique pour la présence du virus. Le résultat de ce test peut être connu, quelques minutes après la prise de l’échantillon.
Le test rapide, dit antigénique, vise à détecter des protéines virales présentes dans un échantillon clinique, servant ainsi de test diagnostique pour la présence du virus. Le résultat de ce test peut être connu, quelques minutes après la prise de l’échantillon.
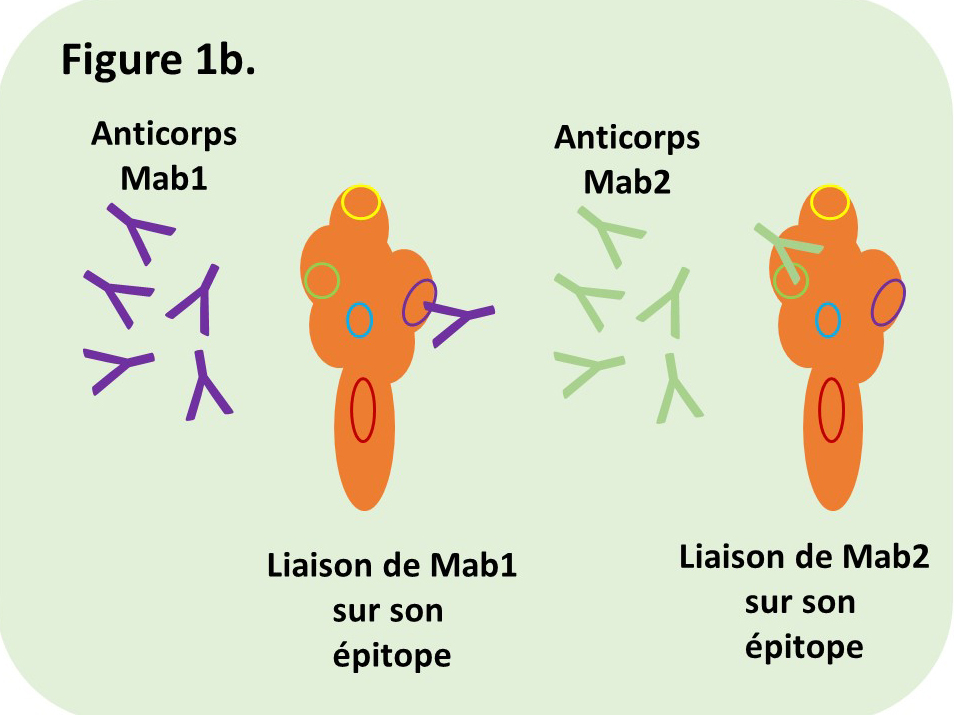
Revenons d’abord aux fondamentaux. Un antigène est une molécule, généralement une protéine. Dans le cadre de la réponse immune celle-ci suscite la montée d’anticorps qui affichent la propriété de la lier spécifiquement et durablement. En fait, les anticorps ne reconnaissent que des petites portions de cette protéine, environ une dizaine d’acides aminés, que l’on appelle épitopes. La protéine affiche toujours plusieurs épitopes. Chacun de ces épitopes, va susciter la montée d’anticorps qui lui est propre (on parle ici essentiellement d’immunoglobulines G, IgG) . Ce mélange d’anticorps reconnait bien toujours la même protéine. On dit de ce mélange qu’il est poly-clonal. En laboratoire, il est possible de produire, à partir de cellules immunitaires de souris infectées, des anticorps qui se lient exclusivement à un seul épitope. Ces anticorps sont dits monoclonaux.
La Figure 1 présente schématiquement une protéine qui affiche cinq épitopes (cercles de différentes couleurs). Dans la partie 1a, cette protéine est recouverte d’un mélange d’anticorps poly-clonaux qui reconnaissent et lient les cinq épitopes. C‘est ce qui se passe généralement dans l’organisme infecté. La partie 1b illustre la liaison d’anticorps monoclonaux (Mab) sur un seul épitope.
Ces précisions apportées, voyons les principes du test. Comme pour le test RT-PCR il faut dans un premier temps avoir accès à une source de matériel que l’on suspecte infecté . Soit du virus, soit des cellules infectées ou leurs débris. Donc, retour à l’écouvillon (cf. Test RT-PCR). Il faut ensuite disposer d’anticorps spécifiques contre une-des protéines virale-es. Pour simplicité, on va évoquer la protéine S du SARS-CoV-2, mais ce test peut tout aussi bien se baser sur une autre protéine virale interne. Ces anticorps sont obtenus par infection d’une espèce animale permissive et produisant une réponse immune efficace. Le sang de ces animaux est récolté et laissé à coaguler. Les anticorps présents dans le sérum sont purifiés et constituent une préparation d’anticorps poly-clonaux spécifiques des antigènes viraux, dont la protéine S. Alternativement, des anticorps monoclonaux peuvent être dérivés en laboratoire, montés contre un seul épitope de la protéine (cf. Figure 1b). Le test consiste maintenant en la mise en évidence du complexe, antigène-anticorps. Dans ce test donc, les anticorps sont connus, ils servent à identifier la présence de la protéine avec laquelle ils forment un complexe stable.
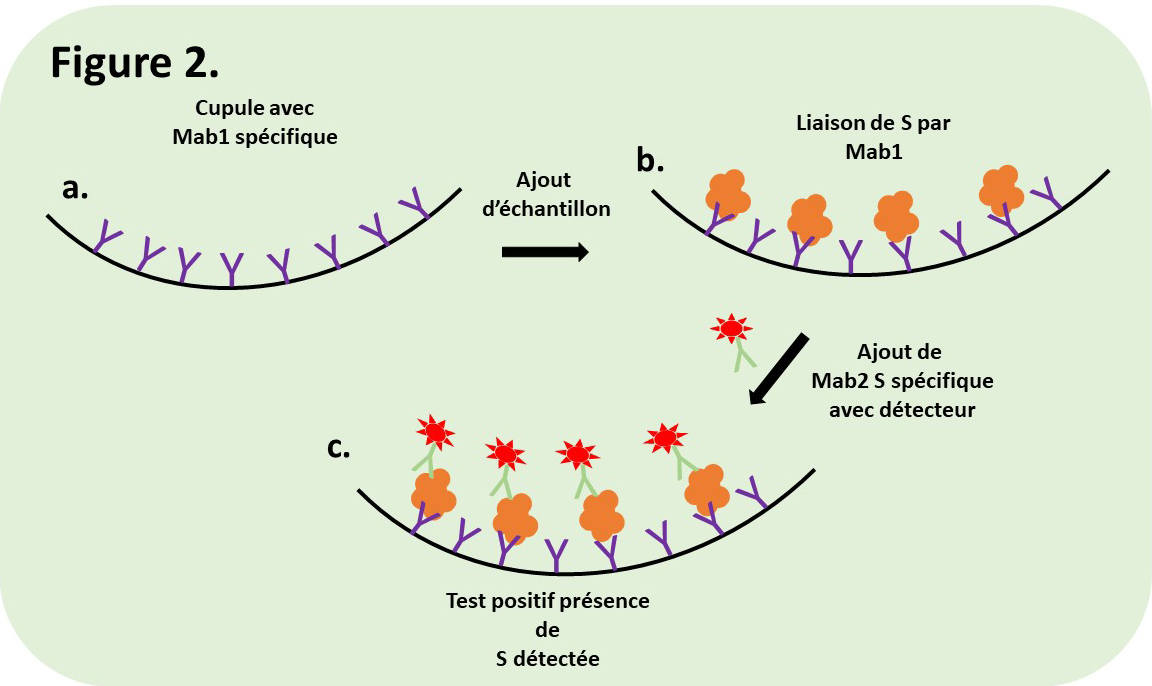
Pratiquement, la préparation d’anticorps est fixée sur un support, le fonds d’une petite cupule de plastique, (cf. Figure 2a.) puis l’échantillon est mis au contact avec ces anticorps. Si la protéine recherchée est présente dans l’échantillon, elle va être retenue, après lavage, par sa liaison avec les anticorps (2b.). Pour mettre en évidence ce complexe antigène-anticorps, une deuxième couche d’anticorps spécifiques est ajoutée. Ces anticorps sont cette fois modifiés pour arborer un signal permettant leur détection (cf. ci-dessous). Après nouveau lavage, la détection de ce signal dans la cupule atteste de la présence de la protéine (c.). La compréhension du test est plus aisée si l’on introduit l’utilisation de deux anticorps monoclonaux différents, pour la fixation de l’antigène et pour la détection. Le signal de détection peut varier. Cela peut être une molécule fluorescente, une enzyme** dont l’activité produit une couleur dans la cupule ou un agent qui est lui-même coloré (or colloïdal).
Munis de ces informations, revenons dans la vraie vie avec le test antigénique à disposition dans certaines pharmacies ( ?) ou dans les laboratoires spécialisés. Ce test se déroule non dans des cupules de plastique mais sur une bandelette de papier buvard (Figure 3.).
L’échantillon est déposé à l’extrémité de la bandelette (a.). Le liquide contenant les protéines virales de l’échantillon migre par capillarité sur la bandelette et rencontre une ligne d’anticorps spécifiques munis d’un détecteur coloré (or colloïdal). Ces anticorps ne sont pas immobilisés, ils sont emportés dans le flux de liquide. Lorsque l’antigène rencontre ces anticorps, le complexe antigène-anticorps se forme et continue sa migration. Il vient buter sur une deuxième ligne d’anticorps anti-protéine virale cette fois fixés au support (b.) La protéine virale liée aux premiers anticorps munis du détecteur vont être retenus sur cette ligne et former une ligne colorée. Les anticorps non complexés avec cette deuxième ligne vont continuer leur migration et buter sur une ligne qui fixe cette fois les anticorps eux-mêmes, qu’ils soient ou non liés avec l’antigène, formant une deuxième ligne colorée. Cette ligne dite de contrôle est le garant de la bonne migration des anticorps sur la bandelette. Elle est toujours visible et sert à certifier le bon déroulement du test (la bonne migration par capillarité). Quant à la première ligne elle n’est visible que si l’antigène a bien été lié au premiers anticorps. En son absence, le test est négatif.
La sensibilité de ce test est limitée par la quantité d’antigène présent dans l’échantillon. Ici, pas d’amplification du matériel viral comme dans le test RT-PCR. En dessous d’une certaine quantité, la première ligne colorée ne sera pas visible. Sa spécificité va dépendre de la spécificité des anticorps et de la singularité des épitopes reconnus. Si des épitopes sont partagés entre plusieurs types de virus, le test ne pourra pas les distinguer. Si les épitopes reconnus n’appartiennent qu’au virus que l’on cherche à identifier alors la spécificité sera très bonne. Les résultats les plus spécifiques seront ceux obtenus avec des anticorps monoclonaux.
 Dans le test antigénique SARS-CoV-2, la probabilité que des anticorps anti-S (ou une autre protéine virale) vont avoir une réactivité croisée avec les autres coronavirus humain est faible. Ces virus affichent moins de 30 % d’identité avec les SARS-CoV-2 (cf. Table 1). En revanche entre la protéine S de SARS-CoV-2 et celle de SARS-CoV, le coronavirus qui a émergé en Asie en 2003, l’identité de séquence est plus élevée. Elle atteint même un 85% dans la partie S2 de la protéine (Figure 4). Cette identité pourrait être problématique pour la spécificité du test dans le cas où les deux coronavirus issus des chauves-souris circuleraient en même temps dans la population humaine, ce qui n’est heureusement pas le cas..en ce moment.
Dans le test antigénique SARS-CoV-2, la probabilité que des anticorps anti-S (ou une autre protéine virale) vont avoir une réactivité croisée avec les autres coronavirus humain est faible. Ces virus affichent moins de 30 % d’identité avec les SARS-CoV-2 (cf. Table 1). En revanche entre la protéine S de SARS-CoV-2 et celle de SARS-CoV, le coronavirus qui a émergé en Asie en 2003, l’identité de séquence est plus élevée. Elle atteint même un 85% dans la partie S2 de la protéine (Figure 4). Cette identité pourrait être problématique pour la spécificité du test dans le cas où les deux coronavirus issus des chauves-souris circuleraient en même temps dans la population humaine, ce qui n’est heureusement pas le cas..en ce moment.
NB. Le déroulement de ce test antigénique, tel que décrit ici, représente un mode de faire basique. Il peut varier avec comme but, généralement atteint empiriquement, d’obtenir la plus grande sensibilité en conservant toutefois la meilleure spécificité.
** Les tests avec comme détecteur une enzyme sont dits tests par ELISA (Enzyme Linked Immunosorbent Assay), que l’on pourrait traduire par test révélé par une « enzyme liée aux anticorps adsorbés ».
Publié 01/12/2021
màj 08/09/2025